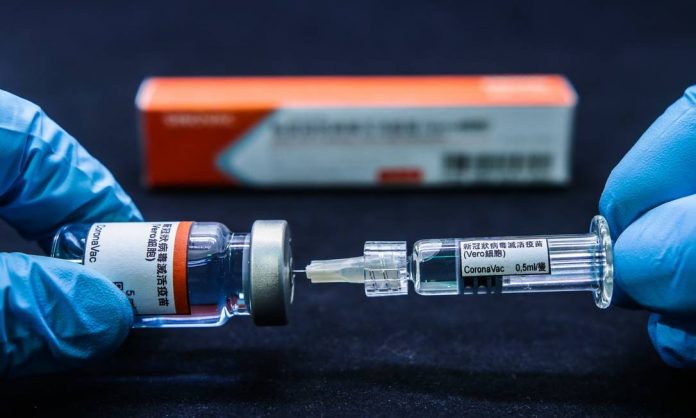
“É a vacina mais segura entre todas as que estão sendo testadas. Ela já foi testada em mais de 70 mil voluntários entre Brasil e China, sendo 15 mil só no Brasil”, disse Covas em entrevista exclusiva ao âncora da CNN Diego Sarza.
Segundo o diretor do Butantan, além dos exames clínicos, é vantajosa ao Brasil a adoção da Coronavac pela semelhança com outras vacinas já produzidas e distribuídas no país. “É uma tecnologia já conhecida. O Butantan domina essa tecnologia e já produz vacinas com ela”, disse.
Dimas Covas afirmou que as contestações pela origem chinesa da Coronavac não se justificam pelo alto número de medicamentos comercializados no Brasil que se utilizam de insumos do país. “A vacina tem o insumo que vem da China, mas hoje esses insumos compõem 80% dos medicamentos vendidos”, disse.
Questionado sobre possíveis atrasos e prazos para que a vacina esteja disponível no país, o diretor do Butantan disse que a programação depende da Agência Nacional de Vigilância Sanitária (Anvisa).
Do total de 46 milhões acertado com a Sinovac, o instituto prevê importar 6 milhões de doses, o que foi autorizado pela Anvisa na sexta-feira (23), e produzir outras 40 milhões localmente. Para isso, é necessária a autorização da agência para a compra dos insumos, o que ainda não ocorreu.
Segundo Dimas Covas, caso “esse processo não demore”, o Butantan pode produzir essas vacinas até um prazo entre o final de dezembro e a primeira quinzena de janeiro de 2021.
Para que as doses sejam utilizadas, também é necessário que a agência autorize o uso no país. Pelos resultados dos testes, o diretor do Butantan espera que isso ocorra até o final deste ano.
Impasse político
Dimas Covas comentou os impasses políticos entre o Butantan e o Ministério da Saúde, que desistiu da intenção de compra da Coronavac e da sua inclusão no Programa Nacional de Imunização. Mais cedo, também em entrevista exclusiva à CNN, o secretário estadual da Saúde, Jean Gorinchteyn, afirmou que o impasse pode atrasar a vacinação no país.
O diretor do instituto afirmou esperar que esse atraso não ocorra, com a inclusão no programa federal acontecendo tão logo a vacina seja autorizada pela Anvisa.
“Com a vacina estando disponível e registrada, haverá maior facilidade de compreensão do Ministério da Saúde e do Programa Nacional de Imunização da necessidade de começar a vacinação, principalmente dos grupos de risco”, disse Covas.
A expectativa do diretor é que as primeiras doses permitam a imunização dos grupos de maior risco para a Covid-19, incluindo idosos, profissionais da saúde, grávidas, puérperas e portadores de comorbidades que agravam os efeitos da doença do novo coronavírus.
Fonte: CNN Brasil